- Autor Stanley Ellington ellington@answers-business.com.
- Public 2023-12-16 00:15.
- Última modificación 2025-01-22 15:57.
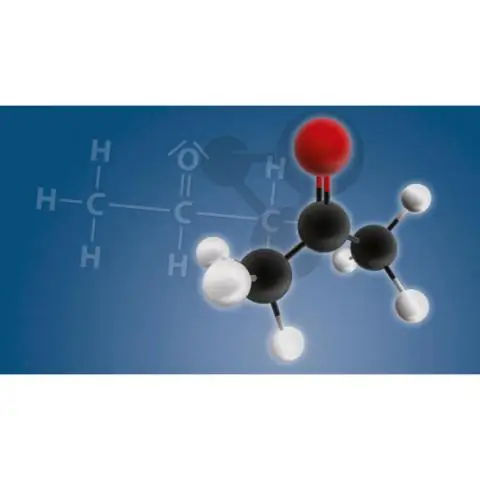
Aldehídos , Cetonas , y Ácidos carboxílicos son compuestos de carbonilo que contienen un doble enlace carbono-oxígeno. Estos compuestos orgánicos son muy importantes en el campo de la química orgánica y también tienen muchas aplicaciones industriales.
En consecuencia, ¿cuál es la diferencia entre un aldehído, una cetona y un ácido carboxílico?
Aldehídos y cetonas contienen el grupo funcional carbonilo. En un aldehído , el carbonilo está al final de una cadena de carbono, mientras que en una cetona , está en el medio. A ácido carboxílico contiene el grupo funcional carboxilo. En un éster, el hidrógeno de un ácido carboxílico El grupo se reemplaza por un grupo alquilo.
¿Cuál es la prueba de identificación de aldehído cetona y ácido carboxílico? Tollens ' Prueba . Tollens ' prueba , también conocido como espejo plateado prueba , es un laboratorio cualitativo prueba utilizado para distinguir entre un aldehído y un cetona.
Además, ¿el aldehído es un ácido carboxílico?
A ácido carboxílico es donde el oxígeno de un éster se une con un hidrógeno. Aldehído es una cetona donde uno de los enlaces del carbono es un hidrógeno. Las aminas se complican porque hay 3 tipos, primaria, secundaria y terciaria. El primero es un grupo NH2.
¿Cuál es el aldehído o el ácido carboxílico más ácido?
Ácidos carboxílicos generalmente tienen pKas en el rango de 3 a 5, y por lo tanto son más débiles ácidos que el ion hidronio (H3O+), pero son más fuertes ácidos que otros orgánicos ácidos , como alcoholes (16 - 20), aldehídos y cetonas (18 - 22), alquinos (25), benceno (35) o alcanos (50).
Recomendado:
¿Qué son los ácidos fuertes y débiles explicados con el ejemplo?

Los ácidos fuertes se disocian (rompen) completamente en agua). Por ejemplo, el HCl, un ácido fuerte, se descompondrá en iones H + y Cl-. Los ácidos débiles se disocian parcialmente en agua. Por ejemplo, el HF, un ácido débil, solo tendrá algunas de las moléculas de HF disociadas en un momento dado
¿Los ácidos débiles tienen un pKa alto o bajo?

001) = -3 entonces pKa = 3. Entonces, cuanto mayor es el pKa, menor Ka, y esto significa un ácido más débil
¿Son ésteres de ácidos carboxílicos?
Un éster de ácido carboxílico es un éster derivado de un ácido carboxílico, que tiene la siguiente fórmula estructural general. Por ejemplo: el grupo O = C - O en un éster de ácido carboxílico se denomina grupo éster de ácido carboxílico. Los ésteres de ácido carboxílico son los ésteres más comunes en química orgánica
¿Por qué los ácidos fuertes tienen un pKa bajo?

Un pKa más bajo significa que el valor de Ka es más alto y un valor de Ka más alto significa que el ácido se disocia más fácilmente porque tiene una mayor concentración de iones de hidronio (H3O +)
¿Por qué los ácidos débiles son débiles?

Un ácido es débil si no todas las moléculas de ácido se ionizan en protones de hidrógeno y su base conjugada en un sistema solvente particular. Alternativamente, si usáramos la definición más amplia de Brønsted, un ácido es débil si no dona completa o casi completamente su protón a alguna base
